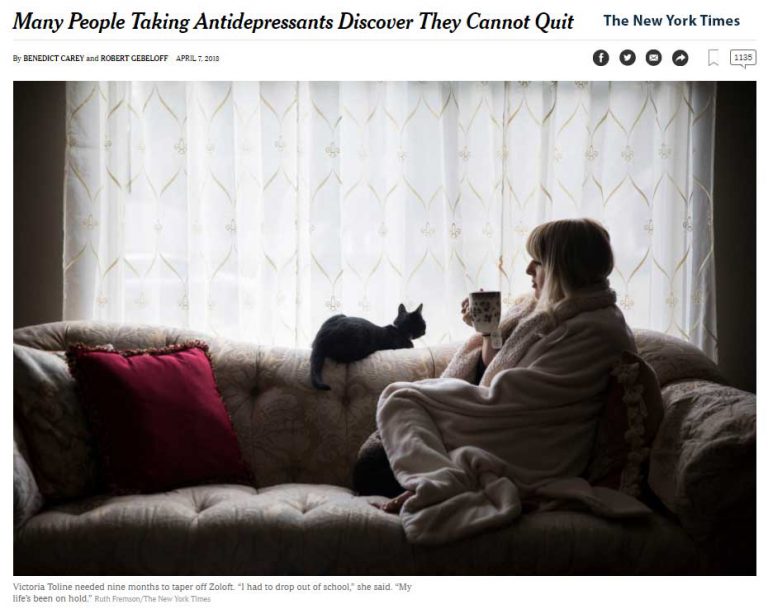
Zusatzinformationen zur S3-Leitlinie Schizophrenie – Methodenkritik: Die Rolle der Neuroleptika
Die neue S3-Leitlinie Schizophrenie ist fertiggestellt und kann hier kostenlos abgerufen werden.
https://www.awmf.org/leitlinien/detail/ll/038-009.html
Einige Aspekte sind in der Leitlinie verkürzt dargestellt und wirken dadurch wie gesicherte naturwissenschaftliche Erkenntnisse, die Naturgesetzen gleichen. Doch genau so funktioniert Wissenschaft nicht und Therapien erst recht nicht. Der Psychiater Volkmar Aderhold hat an der Erstellung der Leitlinie mitgearbeitet, Der Psychiater Stefan Weinmann an einem Methodenpapier der Leitlinie. In diesem Text erklären die beiden auf welcher wissenschaftlichen Datenbasis die Empfehlungen dieser S3-Leitlinie basieren und wie die Empfehlungen (insbesondere zugunsten von Neuroleptika) zustande gekommen sind. Dieser Text warnt vor einer „blinden“ Anwendung der Ergebnisse und rät zu einer sorgfältigen Prüfung nicht nur in Bezug auf die (Langzeit-) Anwendung von Neuroleptika.
Von Dr. Volkmar Aderhold und Dr. Dr. Stefan Weinmann
A. Zur Bedeutung von Leitlinien:
Leitlinien sind nicht bindend.Sie sollen jedoch eine starke Orientierung geben, weil sie den aktuellen Stand der Wissenschaft, insbesondere die Ergebnisse von randomisierten Studien und den Konsensus der eingeladenen nationalen Expertenrunde aus vielen Berufsgruppen und Betroffenen und Angehörigen (zu wenige) wiedergeben. Es gibt sie auch für viele Erkrankungen der somatischen Medizin.
Kommt es zu Klagen und Prozessen, berücksichtigen Gerichte bei ihrer Urteilsfindung heute immer mehr diese Leitlinien und wollen von Sachverständigen wissen, ob eine Praxis von den Leitlinien abgewichen ist.
Weichen Ärzte in ihrer Praxis von Leitlinien ab, insbesondere bei der Pharmakotherapie wegen des Risikos einer Schädigung, sind sie gehalten, die Patienten darüber aufzuklären. Daher müssen Verfahren zur angemessenen und verständlichen Aufklärung von Menschen mit schweren Beeinträchtigungen und ihren Angehörigen entwickelt werden, auch wissenschaftlich und unter Einbeziehung von Psychiatrie-Erfahrenen. Dass dies bisher nur unzureichend erfolgt ist, kann nicht als Rechtfertigung dazu dienen, Menschen unzureichend aufzuklären und Antipsychotika unter Verweis auf methodisch fragwürdige Studien als alternativlos darzustellen.
Wurde ein Patient jedoch zu den kurz- und langfristigen Risiken von Antipsychotika nicht aufgeklärt, kommt es im Klagefalle zu Beweiserleichterungen bis hin zur Beweislastumkehr: Dann muss nicht mehr der klagende Patient nachweisen, dass er geschädigt wurde, sondern der Behandelnde, dass er dies mit einer abweichenden Praxis nicht verursacht hat.
Wir möchten daher zur Frage der Wirksamkeit noch Ergänzendes hinzufügen. Dies ist ein Beispiel dafür, wie wir anhaltend durch methodisch komplexe Publikationen getäuscht werden.
B. Wirkmechanismus der sogenannten Antipsychotika:
Neuere bildgebende Verfahren lieferten Daten, die bei Menschen mit psychotischen Symptomen einer präsynaptischen Überaktivität der dopaminergen Bahnen im Streifenkern entsprechen, einer Struktur unterhalb des Großhirns. Dies entspricht dem Erklärungsmodell, dass „Schizophrenie“ mit einer Hyperaktivität der subkortikalen Übertragung von Dopamin an D2-Rezeptoren verbunden ist. Darüber hinaus deuten diese Ergebnisse darauf hin, dass diese dopaminerge Überaktivität subkortikaler Systeme episodischer Natur ist, also nur während einer psychotischen Episode besteht und nur einige Aspekte der Positivsymptomatik ausmacht (Guillin et al 2007).
Zugleich sind diese Veränderungen nur mit Positiv-, jedoch kaum mit Negativ- und nicht mit kognitiven Symptomen verbunden.
Und es gibt auch eine Patientengruppe mit psychotischen Symptomen, bei der diese Überaktivität gering oder gar nicht nachweisbar ist. Im Rahmen dieser Logik können sie daher auch nur gering oder sogar gar nicht auf die Antipsychotika ansprechen (Howes et al 2012).
Da solche Veränderungen an den Rezeptoren nicht nur genetisch sondern in vielfältiger Weise epigenetisch, also durch Umweltfaktoren bedingt sind, die diese genetischen Faktoren erst krankheitsrelevant werden lassen, ist mittlerweile hinlänglich belegt. (Howes & Murray 2014)
Antipsychotika sind hingegen Substanzen, die den Dopaminrezeptor (insbesondere eine Untergruppe, den D2/3 Rezeptor) nur postsynaptisch hemmen und damit diese subkortikale dopaminerge Anormalität nicht gezielt rückgängig machen können, sondern nur auf die Folgen einwirken. Leider führen sie dadurch auch oft zu einer Zunahme (upregulation) dieser blockierten Dopaminrezeptoren, denn eine vermehrte Anzahl ist bei unbehandelten Patienten mit erster Episode nicht, jedoch häufig später nach Behandlungen nachzuweisen.
Hinzu kommt eine dosisabhängige Super-Sensibilisierung der Dopamin-Rezeptoren im Streifenkern als Anpassung an der Eingriff durch Antipsychotika. Tierexperimentell kommt es zu einer Verdreifachung der Dopaminrezeptoren im „D2-High State“ nach Gabe von Antipsychotika. Dadurch entsteht an diesen Rezeptoren eine erhöhte Empfindlichkeit für Dopamin. Ein Nachweis ist bisher jedoch nur in Tierexperimenten möglich (Seemann et al 2005 und 2006; Samaha et al. 2008).
Nicht sicher ist, ob diese negativen Hirnveränderungen bei jedem Behandelten und bei jeder Substanz gleich auftreten. Auch ist nicht sicher, wie lange sie nach dem Absetzen noch anhalten. Man geht aufgrund tierexperimenteller Daten von mehr als einem Jahr beim Menschen aus (Murray et al 2016), bis hin zu mehreren Jahren und potentiell auch von Irreversibilität (Chouinard et al 2008).
Damit besteht beim Absetzen von Antipsychotika eine erhöhte Rezeptorverfügbarkeit, und diese Supersensitivität kann Absetzphänomene und ein erhöhtes Rückfallrisiko bedingen (Howes et al 2012). Diese Phänomene sind in der Methodik der bisherigen Medikamentenstudien nur unzureichend berücksichtigt, so dass viele Studien zur Wirksamkeit von Antipsychotika verfälscht sind.
Des Weiteren konnte durch bildgebende Verfahren darauf hindeuten, dass ein Defizit bei der dopaminergen Übertragung im präfrontalen Kortex an der Entstehung kognitiver Symptome von Patienten mit Schizophrenie beteiligt ist (Guillin et al 2007). Da Antipsychotika jedoch nicht nur auf die subkortikale Region einwirken, also nicht selektiv sind, können sie damit auch zu einer Verschlechterung von Negativ- und kognitiven Symptomen führen (Howes et al 2012).
Und weil Antipsychotika Fremdmoleküle sind, die auch noch ganz andere Rezeptorgruppen blockieren können, kommt es zu den weiteren bekannten Nebenwirkungen.
C. Zur Wirksamkeit der Antipsychotika bei Ersterkrankten und Mehrfacherkrankten
„Prinzipiell ist zu beachten, dass keine Studien bei ersterkrankten Patienten verfügbar sind, die die Wirksamkeit eines Antipsychotikums mit Plazebo vergleichen.“ So die Langfassung der Leitlinien auf S. 69.
In einer Cochrane Metaanalyse von 2011 wurden hingegen 5 Studien gefunden und ausgewertet. (Bola et al 2011) Hier das Ergebnis:
„Mit nur wenigen Studien, die die Einschlusskriterien erfüllen, und mit begrenzten verwertbaren Daten in diesen Studien ist es nicht möglich, endgültige Schlussfolgerungen zu ziehen. Das vorläufige Evidenzmuster deutet darauf hin, dass Menschen mit Schizophrenie in einer frühen Episode, die mit typischen Antipsychotika behandelt wurden, die Studie mit geringerer Wahrscheinlichkeit vorzeitig verlassen, jedoch häufiger medikamentenbedingte Nebenwirkungen haben. Die Daten sind zu spärlich, um die Auswirkungen von Antipsychotika auf die Ergebnisse bei Schizophrenie in frühen Episoden beurteilen zu können. “ [“With only a few studies meeting inclusion criteria, and with limited useable data in these studies, it is not possible to arrive at definitive conclusions. The preliminary pattern of evidence suggests that people ewith early episode schizophrenia treated with typical antipsychotic medications are less likely to leave the study early, but more likely to experience medication-related side effects. Data are too sparse to assess the effects of antipsychotic medication on outcomes in early episode schizophrenia.”]
In einem 2019 veröffentlichten systematischen Review zu placebokontrollierten Studien zu Antipsychotika bei unbehandelten Menschen mit Psychosen (Danborg & Gøtzsche 2019) finden die Autoren noch eine neuere Studie (Wang et al 2013) und kommen zu dem Ergebnis: „Es war eine chinesische Studie, in der Olanzapin und Placebo bei 261 Patienten mit einer ersten Episode einer Schizophrenie verglichen wurden. Nach 12 Wochen gab es einen extrem großen Unterschied zugunsten von Placebo, aber die Autoren berichteten das Gegenteil, dass Olanzapin wirksam war. “ [„It was a Chinese trial comparing olanzapine with placebo in 261 patients with first-episode schizophrenia. After 12 weeks, there was an extremely large difference favouring placebo, but the authors reported the opposite, that olanzapine was effective.“]
Zur Wirksamkeit der Antipsychotika bei mehrfach Erkrankten zitieren die Leitlinien auf S. 70 eine Metaanalyse aus dem Jahr 2017:
„Eine Meta-Analyse hat alle randomisierten und plazebokontrollierten Studien zur Wirksamkeit von Antipsychotika bei Menschen mit einer Schizophrenien von 1955 (1953: Einführung des Chlorpromazins) bis 2016 untersucht und konnte 167 Studien mit 28.102 Teilnehmern identifizieren (185). Diese Analyse berücksichtigte keine Studien, die ausschließlich ersterkrankte Patienten oder Patienten mit einer pharmakologischen Behandlungsresistenz eingeschlossen hatten, da solche Studien mit dem hier geforderten Design nicht verfügbar sind. 42% der Studien waren durch den Hersteller des jeweiligen Präparats finanziert, 43% waren nicht durch die Industrie gesponsert und 15% machten keine Angaben in Bezug auf die Finanzierung (185). Die mittlere Effektstärke über alle Studien zusammen war 0,47, und Patienten, die auf ein Antipsychotikum randomisiert worden waren, respondierten doppelt so häufig wie Patienten, die auf ein Plazebo randomisiert worden waren (NNT = 6). 51% der Patienten mit Antipsychotikabehandlung und 30% der Patienten unter Plazebo erfuhren eine minimale Response (≥ 20% Verbesserung der Psychopathologie in PANSS/BPRS) (NNT = 5) (185). 23% der Patienten mit Antipsychotikabehandlung und 14% der Patienten unter Plazebo zeigten eine gute Response (≥ 50% Verbesserung der Psychopathologie in PANSS/BPRS) (NNT = 8) (185). Unter Antipsychotika (13%) gab es weniger Therapieabbrüche in den Studien als unter Plazebo (26%) (NNT = 7). Während der Antipsychotikabehandlung traten mehr motorische Nebenwirkungen (NNH = 12), mehr Sedierungen, mehr Gewichtszunahmen, mehr Prolaktinanstiege und mehr QTc- Verlängerungen auf (185). Weiterführende Moderatoranalysen zeigten, dass die Effektivität von Plazebo in den letzten 60 Jahren kontinuierlich gestiegen ist, während die Effektivität der Antipsychotika gleich geblieben ist (185).“ (Leucht et al 2017)
Darin kommen die Autoren zu dem Ergebnis:
„43% waren nicht durch die Industrie gesponsert …Die mittlere Effektstärke über alle Studien zusammen war 0,47, und Patienten, die auf ein Antipsychotikum randomisiert worden waren, respondierten doppelt so häufig wie Patienten, die auf ein Placebo randomisiert worden waren (NNT = 6).“ Jedoch nur, wenn jedes berichtete Responsekriterium in die Auswertung einbezogen wurde.
„51% der Patienten mit Antipsychotikabehandlung und 30% der Patienten unter Plazebo erfuhren eine minimale Response (≥ 20% Verbesserung der Psychopathologie in PANSS/BPRS) (NNT = 5)“.
Der Unterschied in der minimalen Responserate unter Neuroleptika gegenüber den Placebo-Gruppen beträgt in dieser Metaanalyse demnach 21 % und die Anzahl der erforderlichen Behandlungen (NNT), um einen im Vergleich mit der Placebobehandlung besseren Response-Effekt zu erzielen, beträgt 5.
„23% der Patienten mit Antipsychotikabehandlung und 14% der Patienten unter Plazebo zeigten eine gute Response (≥ 50% Verbesserung der Psychopathologie in PANSS/BPRS) (NNT = 8).“
Damit konnte im Vergleich mit der Placebogruppe nur bei weiteren 9% der Vorteil einer Reduktion der Symptomatik von mindestens 50% festgestellt werden. Dieses Ergebnis wurde allerdings nur in 14 der insgesamt 167 Studien erhoben und ergab bei der Subgrupppenanalyse dieser Studien lediglich eine NNT von 10. (Leucht et al 2017, Suppl. S. 72) Erst durch die metaanalytische Neuberechnung ermitteln die Autoren eine NNT von 8.
Aber sind diese Aussagen so gerechtfertigt? Da es sich (neben der Netzwerk-Meta-Analyse placebokontrollierter Studien vom selben Autorenteam (Leucht et al. 2013) um die einzige in den Leitlinien zur Wirksamkeit von Neuroleptika ausgeführte Metaanalyse placebokontrollierter Wirksamkeitsstudien handelt, soll sie genauer beleuchtet werden, denn solche Metaanalysen sind ein Teil des Problems.
Hier zunächst eine kurze Zusammenfassung des Ergebnisses, danach die dazu führende Methodenkritik:
Durch notwendige Korrekturen aufgrund von erheblichen methodischen Mängeln der ausgewerteten Studien verringert sich die minimale Response (niedrigste klinische noch bedeutsame Symptomreduktion) von 51 % auf nur etwa 38%.
So sinkt der Anteil der Menschen, der tatsächlich und auch nur geringfügig von Neuroleptika profitiert, auf etwas mehr als ein Drittel (38%) mit einer NNT von 6. Und nur bei weniger als einem Viertel (23%) der Behandelten zeigt sich eine Symptomreduktion um 50 % mehr, was angesichts der Placeborate lediglich eine NNT von 10 bedeutet.
Dabei ist die NNT (‚number needed to treat‘) – die Anzahl der notwendigen Behandlungen – eine statistische Maßzahl, die angibt wie viele Patienten pro Zeiteinheit (hier durchschnittlich 6 Wochen, länger wurden die Studien im Mittel nicht durchgeführt und in diesem Zeitraum betrug durchschnittliche Abbruchquote 37 %) mit dem Medikament behandelt werden müssen, um das gewünschte Therapieziel bei einem Patienten zu erreichen.
Hinzu kommen weitere Einschränkungen, die in der Art der durchgeführten Studien bedingt sind. Diese schwächen diese Ergebnisse weiter ab, können jedoch nicht statistisch umgerechnet werden.
Das Angebot von ersetzenden und ergänzenden psychosozialen Behandlungsformen ist daher dringend geboten und ebenfalls ihre Beforschung.
Liest man die gesamte Publikation und das ergänzende Material genauer, so stößt man auf bedeutsame weitere Einschränkungen im Leitlinientext gemachten Aussage.
Folgende Punkte sind für die Beurteilung von Wirkungen und Nebenwirkungen von Antipsychotika in den Studien der Metaanalyse von Bedeutung:
(1) Die Metaanalyse selbst berichtet von diversen methodischen Einschränkungen, sodass die Effektstärke SMD (standardized mean difference) aufgrund der Verzerrung infolge kleiner Studien sowie nicht publizierter Studien mit schlechten Effekten von d = 0.47 auf 0.38 nach unten korrigiert werden musste. [“but accounting for small-trial effects and publication bias reduced the SMD to 0.38.”] Damit ist die Effektstärke schon mal um 20% geringer und nicht mehr mittelgradig, denn das wäre sie erst ab d=0,5. Diese korrigierte Effektstarke wird jedoch im Leitlinientext nicht erwähnt. Sie ist damit nicht mehr mittelgradig.
(2) Und die von der Industrie gesponserten Studien (57%) hatten im Durchschnitt eine um 0,16 geringere Effektstärken im Vergleich zu den nicht von der Industrie gesponserten Studien (Tabelle 3). [“industry-sponsored studies, on average, had a 0.16 smaller effect size compared with non-industry-sponsored trials (Table 3).” Ein “statistisch signifikanter Moderator” (Tab 3.) Und trotzdem werden die gesamten weiteren Berechnungen in der Publikation ohne diese Korrekturfaktoren durchgeführt.
(3) Und was bedeutet eine „minimale Response von ≥ 20% Verbesserung der Psychopathologie in PANSS/BPRS“? In der Publikation steht dazu: „Mehrere Analysen zeigten, dass eine Reduktion von 20% PANSS/BPRS ungefähr einer minimalen Verbesserung des CGI … entsprach,“. Der CGI ist eine Skala bei der eine minimale Verbesserung die geringste Stufe einer klinisch bedeutsamen Symptomreduktion darstellt.
Aber stimmt das? Was verbirgt sich hinter dem Wort “ungefähr“ [“robustly“]?
Erst auf S. 7 der Publikation ist zu lesen: „Die mittlere Effektgröße für die Gesamtsymptome (0,47) war laut Cohen (61) nur mittelgroß und entspricht einer Differenz von 9,6 PANSS-Punkten.“ [„The mean effect size for overall symptoms (0.47) was only medium according to Cohen (61), and it translates to a difference of 9.6 PANSS points.“] Nun lag die korrigierte Effektstärke nur noch bei 0.38 und damit beliefe sich die PANSS Reduktion nur noch auf 7,8 Punkte.
Wie ist eine Symptomreduktion um 9,6 bzw. 7,8 PANSS Punkte zu bewerten?
In einer methodenkritischen Publikation schreibt Prof. Leucht u.a. selbst, dass erst ein „PANSS um ungefähr 15 Punkte einem CGI-C von ‚minimal verbessert‘ entspricht“ (Leucht et al 2006). Eine minimale Verbesserung auf der Skala für den klinischen Gesamteindruck (Clinical Global Impression) entspricht damit etwa 10 Punkten auf der BPRS-Skala und 15 Punkten auf der PANSS-Skala.
Daher kommt er in dieser Publikation auch zu dem Ergebnis, dass erst PANSS Reduktion um 25% (Bereich 24 –28) eine Reduktion im CGI um eine Stufe widerspiegeln würde.
In der vorliegenden Metaanalyse behauptet er jedoch: „Mehrere Analysen zeigten, dass eine Reduktion von 20% PANSS/BPRS in etwa einer minimalen Verbesserung des CGI …. entsprach“ [„Several analyses showed that a 20% PANSS/BPRS reduction roughly corresponded to minimal improvement on the CGI”].
So wird also behauptet, 9,6 Punkte wären ungefähr 15 Punkte und 20% Symptomreduktion sei ungefähr 25%.
Tatsächlich liegt der errechnete Effekt also nur bei ungefähr der Hälfte der geringsten Stufe eines als klinisch bedeutsam anerkannten Effektes (7,8 von 15 PANSS Punkten).
Wäre also die tatsächliche Höhe der durchschnittlichen PANSS-Reduktion als Responsekriterium gewählt worden, wie er selbst in seinen methodenkritischen Publikationen vorschlägt, wäre die NNT deutlich schlechter als 6.
In der methodenkritischen Publikation geht er sogar noch weiter: „Akut kranke, nicht refraktäre Patienten mit Schizophrenie sprechen in der Regel gut auf Antipsychotika an. Wir schlagen daher vor, dass in solchen Populationen der Cutoff-Wert um mindestens 50% BPRS / PANSS-Reduktion (was „viel Besserung“ widerspiegelt) informativer sein könnte.“ (Leucht et al 2006)
Legt man diesen Maßstab an (der, in der Annahme, Ersterkrankte respondieren besser auf Antipsychotika, auf Ersterkrankte zielen soll), so hätten also nur zusätzliche 9% der antipsychotisch Behandelten einen Symptomminderungseffekt um die Hälfte im Vergleich mit der Placebogruppe. In der Meta-Analyse von Leucht waren keine Studien mit ausschließlich Ersterkrankten, aber Studien eingeschlossen, in denen neben Mehrfach- Erkrankten auch Ersterkrankte teilnahmen.
Wir können kann diese verzerrende Darstellung in der Metaanalyse nicht anders als einen bewussten Täuschungsversuch auffassen, ein Versuch, die sehr enttäuschende Bilanz zu beschönigen, um den möglichst breiten Einsatz von Neuroleptika zu rechtfertigen.
Denn die Autoren fassen in der „Schlussfolgerung“ der Metaanalyse beruhigend zusammen: „Erstens können die Kliniker erwarten, dass sich bei der Behandlung mit Antipsychotika im Vergleich zu Placebo etwa zweimal mehr Patienten bessern, jedoch nur eine Minderheit wird eine gute Response in kurzer Zeit erfahren. [„First, clinicians can expect that approximately two times more patients improve when treated with antipsychotics compared with placebo but only aminority will experience a good response in the short term.“]
(4) Hätten Leucht et al noch genauer zwischen älteren (1991-1998) und neueren Studien (1999-2008) unterschieden, so wären die Ergebnisse noch weitaus ernüchternder gewesen. Dies nämlich haben Khin et al von der FDA, der amerikanischen Zulassungsbehörde in einer Publikation von 2012 gemacht. Darin haben sie für diese Zeiträume die jeweiligen Mittelwerte des PANSS-Gesamtscore der Differenz zwischen Placebo und Medikation errechnet. So ermittelten sie in den neueren Studien ab 1999 einen Abfall von 10.8 (was ja bereits schon deutlich weniger ist als eine Stufe im CGI) auf 6.0 für nordamerikanische Studien bzw. 7.2 bei Auswertung aller Studien, also nur noch etwas mehr als ein Drittel der geringsten klinisch bedeutsamen Stufe. Das es sich ausschließlich um Zulassungsstudien für neuere Antipsychotika gehandelte, die bei der Zulassungsbehörde eingereicht wurden, ist von einer im Vergleich recht guten Studienqualität auszugehen. Die Autoren schlussfolgern: „Eine hohe und zunehmende Placebo-Response und ein abnehmender Behandlungseffekt sind in den Schizophrenie-Studien in Nordamerika von großer Bedeutung. In dieser Ära von globalen klinischen Studien ist dem Design und der Durchführung dieser Studien besondere Aufmerksamkeit zu widmen.“ [Conclusions: A high and increasing placebo response and a declining treatment effect are of great concern in schizophrenia trials conducted in North America. In this era of global clinical trials, close attention is needed to the design and conduct of these trials.“] Auch macht der kontinuierliche historische Anstieg des Placeboeffektes bis heute, eine bessere Wirkung als Placebo von neueren Studien unwahrscheinlich.
(5) Dabei repräsentiert die sog. Placebo-Wirkung den gesamten psychosozialen Kontext, in dem eine Behandlung stattfindet. Verbessert er sich, sind insgesamt verbesserte Behandlungsbedingungen bei neueren Studien anzunehmen. Da sie in den Studien jedoch nie den Charakter einer echten Psychosebegleitung haben, ist anzunehmen, dass der Placeboeffekt noch gar nicht ‚ausgeschöpft‘ ist. Die Abbruchquote ließe sich so auch vermindern und der Zeitraum für eine Rückbildung der Symptome, der meist 6 Wochen und länger beträgt, durch eine längere Studiendauern besser ausschöpfen.
Damit würde sich die NNT für Neuroleptika, um dem Placeboeffekt überlegen zu sein, noch erhöhen, das heißt > 6 sein.
Stattdessen empfehlen Leucht et al 2017: „Zur Verbesserung der Signalerkennung in placebo-kontrollierten Studien müssen sich die Forscher darauf konzentrieren, die Reaktion auf Placebo zu reduzieren, anstatt die Reaktion auf Medikamente zu erhöhen. [“To improve signal detection in placebo controlled trials, researchers need to focus on reducing placebo response rather than on increasing drug response.”]
Wäre es nicht weit besser aus der zunehmenden Placebo-Response abzuleiten und zu lernen, wie sie im klinischen Alltag gut genutzt werden kann?
Bezüglich des Placebo-Effektes sind in diesem Zusammenhang auch tierexperimentelle Befunde interessant: Wiederholte, negativ erlebte Umweltstimuli bei der Verabreichung eines Arzneimittels können durch Konditionierung kompensatorische Reaktionen hervorrufen, wodurch die Wirksamkeit des Arzneimittels verringert wird und sich das Risiko nachteiliger Nebenwirkungen erhöht. Unterstützende Umwelteinflüsse wirken meist umgekehrt. (Rief et al 2016).
Diese Tendenz der ständig fallenden Placebo-Verum-Differenz in den Antipsychotika-Studien war natürlich auch Forschergruppe um Leucht bekannt. Wie tief wäre der PANSS-score in der vorliegenden Metaanalyse von Leucht et al abgesunken, hätte man nur die neueren Studien berücksichtigt? Die Empfehlung am Ende der Metaanalyse von 2018 kleinere Studien zu machen, ist grotesk: „Wir empfehlen etwas kleinere Studien mit besser ausgewählten Patienten, um diesen Trend umzukehren.“ [“We recommend somewhat smaller studies, but with better selected patients, to reverse this trend.“] Zitieren die Autoren doch selbst eine Studie, die das kritisiert: „Evidenz basierend auf einer kleinen Anzahl randomisierter Probanden sollte vorsichtig interpretiert werden. Die frühere Wirksamkeit von Pharmakotherapien wird gelegentlich überschätzt. [„Evidence based on a small number of randomized subjects should be interpreted cautiously. Early treatment efficacy of pharmacotherapies is occasionally overestimated.“] (Trikalinos et al 2004) Leucht et al gehen es wohl darum, einen historischen Trend zu stoppen, aber nicht darum bessere Studien und Metaanalysen zu machen. Kleinere Studien mit höherer Selektion der Teilnehmer hätten noch weniger ‚externe Validität‘ d.h. Aussagekraft für andere Patienten.
(6) Aber es kommen noch weitere methodische Einschränkungen und Täuschungen dazu:
Im Jahr 2009 veröffentlichte Prof. Leucht mit einer weitgehend anderen Autorengruppe eine Metaanalyse zu der gleichen Fragestellung. In der Zusammenfassung wird formuliert:
„Wir haben eine systematische Überprüfung und Metaanalyse randomisierter kontrollierter Studien durchgeführt, in denen Antipsychotika der zweiten Generation (SGA) mit Placebo bei schizophrenen Patienten verglichen wurden und die 13 verschiedene Endpunkte berücksichtigten. 38 randomisierte kontrollierte Studien mit 7323 Teilnehmern wurden eingeschlossen. Alle SGA-Medikamente waren wirksamer als Placebo, aber die gepoolte Effektgröße (ES) für die Gesamtsymptome (primärer Endpunkt) war moderat (- 0,51). Die absolute Differenz (RD) in den Responder-Raten lag bei 18% (41% sprachen auf das Medikament an, verglichen mit 24% auf das Placebo, erforderliche Anzahl zur Behandlung = 6).“
[“We conducted a systematic review and meta-analysis of randomized controlled trials that compared second-generation antipsychotic (SGA) drugs with placebo in schizophrenic patients and which considered 13 different outcome measures. Thirty-eight randomized controlled trials with 7323 participants were included. All SGA drugs were more effective than placebo, but the pooled effect size (ES) for overall symptoms (primary outcome) was moderate (- 0.51). The absolute difference (RD) in responder rates was at 18% (41% responded to drug compared with 24% to placebo, number needed to treat = 6).”]
In dieser Metaanalyse von 2009 wurde also nur eine Placebo-Neuroleptika-Differenz von tatsächlich 17 % ermittelt und die NNT betrug 6, im Gegensatz zu den 21% und der NNT von 5 in der in den Leitlinien ausgeführten Metanalyse von 2017. Auch in dieser Publikation steht auf S. 12 im Volltext: „Wir haben die neueren Studien, die den PANSS benutzten, gemeinsam ausgewertet und haben einen Unterschied von 10 Punkten in der PANSS gefunden. Gemäß Leucht et al (2006a) spiegelt ein PANSS mit einem Gesamtscoreunterschied von 15 Punkten eine minimale Verbesserung gemäß dem CGI wider.“ [We pooled the more recent studies using the PANSS and found a difference of 10 points. According to Leucht et al., a PANSS total score difference of 15 points reflects minimal improvement according to the CGI.“]
Wie ist dieser Unterschied zwischen der Metaanalyse von 2017 und 2009 zu erklären? Es wurden in dieser Metaanalyse von 2009 vor allem Zulassungsstudien bis Sept. 2006 ausgewertet, und fast alle wurden von der Pharmaindustrie durchgeführt. Da sie für die Erlangung einer Zulassung bestimmt und ausgewählt worden waren, hatten sie sicher einen möglichst guten Effekt, also eine relativ hohe Placebo-Verum-Differenz. Studien mit einer geringeren Differenz werden oft gar nicht erst publiziert. (sog. Studien in der Schublade bzw. ‚industry bias‘). Weil alle ausgewerteten Studien älter waren und unter den Wissenschaftern weitgehende Einigkeit darüber besteht, dass auch nach 2009 ein immer weiteres Ansteigen der sog „Placeboresponse“ und damit Verringerung des Plazebo-Verum-Differenz stattgefunden hat [„a trend that has not been stopped by the most recent antipsychotics brexpiprazole and cariprazine“], müsste sich die ermittelte Wirkung der Neuroleptika eigentlich weiter verringern. Darum ist der Anstieg der Differenz als die Zunahme der Wirksamkeit und die Abnahme der der NNT von 6 auf 5 in der Metaanalyse von 2017 umso erstaunlicher. Grund dafür ist ein methodisches ‚Kunststück‘ dass der Forschergruppe um Prof. Leucht hier gelingt: zwar steigt der Plazebo-Effekt um 6% an, mehr jedoch der Effekt der Neuroleptika um 10%. Wie ist das möglich?
Schaut man in dem ergänzenden Material, in dem die in der Metaanalyse von 2017 ausgewerteten Studien nur zu finden sind, und vergleicht sie mit den eingeschlossenen Studien der Metaanalyse von 2009, so fällt auf, dass 14 der 38 Studien der Metaanalyse von 2009 in der Metaanalyse von 2017 gar nicht eingeschlossen wurden. Gleichzeitig werden jedoch aus den Jahren vor 2006 – dem Recherchezeitraum der Publikation vor 2009 – 92 weitere Studien eingeschlossen, von denen 75 gemäß der eigenen Bewertung der Autoren (Tab. S5a im ergänzenden Material) von nachgewiesener schlechter oder nicht nachvollziehbarer Qualität sind.
Zur Qualität der Studien und zur Studiendarstellung schreiben die Autoren zusammenfassend in der Publikation: „In den Berichten wurden jedoch häufig nicht alle Details zur Sequenzgenerierung oder zum Verbergen der Zuordnung angegeben. Auch die Beschreibung der Methoden und des Erfolgs der Verblindung reichte häufig nicht aus. Die Daten bestätigten die hohen Abbrecherquoten in aktuellen Schizophreniestudien (Mittelwert 37,2%, SD 20,5). Ältere Studien wurden nur unzureichend wiedergegeben, sodass es oft unmöglich ist, Ergebnisdaten zu extrahieren (50% der Studien hatten ein hohes Risiko für selektive Meldungen).“ [„but the reports often did not indicate full details about sequence generation or allocation concealment. Descriptions of the methods and success of blinding were frequently insufficient as well. The data confirmed the high dropout rates in current schizophrenia studies (mean 37.2%, SD 20.5). Older studies were poorly reported, making it often impossible to extract outcome data (50% of the studies had a high risk of selective reporting).”] Es sind Studien an „vorwiegend chronischen Patienten“ mit einer durchschnittlichen Studiendauer von 6 Wochen. Es wurden diesmal auch alle Studien eingeschlossen, die nur irgendein Ergebnis mitgeteilt haben, so waren es insgesamt 97 Studien. Sie mussten also keine Aussage treffen über das eigentlich wichtige Ergebnis: die Symptomreduktion. So belief sich die Anzahl der Studien, die Werte zu einer minimalen Symptomminderung veröffentlichten, nur auf 46 Studien. Es ist jedoch zweifelhaft, ob Studien zur Wirksamkeit von Neuroleptika in der Akutbehandlung, die keine Daten zur Symptomreduktion messen oder veröffentlichen, eine ausreichende Qualität besitzen. Werden solche Studien trotzdem publiziert, so ist mit hoher Wahrscheinlichkeit von einem ‚reporting bias‘ auszugehen. So zeigt auch eine genauere Übersicht über die Qualität der einzelnen Studien, dass die Hälfte ein hohes Risiko für eine selektive Mitteilung von Daten aufwies (selective reporting/reporting bias) (Ergänzendes Material [supplemental material] S. 70) Es werden dann nur die Daten veröffentlicht, die günstig aussehen. Die Publikation solcher Studien dient meist nur dem Marketing: irgendein Ergebnis wird publiziert, um damit die Verordnung dieser Substanz zu bewerben. Es kann daher angenommen werden, dass die meisten dieser Studien bezüglich der Symptomminderung schlechte Ergebnisse ermittelten, die somit nicht in die Auswertung der Metaanalyse eingegangen sind und sicher das Gesamtergebnis geschmälert hätten, denn immerhin war es die Hälfte der Studien. Zwischen 48% und 57 % der Studien waren von der Pharmaindustrie finanziert. Die Industrie kann dann meist auch entscheiden, welche Daten veröffentlicht werden und welche nicht. Dies wurde auch als ein entscheidender Einflussfaktor auf die Ergebnisse metaanalytisch ermittelt. Dies wird jedoch nur lapidar mitgeteilt, ohne jedoch diesen Faktor bei der Auswertung zu kontrollieren.
(7) Und welche antipsychotischen Substanzen werden in den neueren Studien ab 2006 ausgewertet? Es wurden auch Studien an neuen Substanzen, meist sog. Phase 2 und 3 Studien vor einer Zulassung eingeschlossen. In der Publikation selbst heißt es zu Anzahl der jeweiligen Studien nur: „for all other drugs, fewer than five studies were available.“ Welche Substanzen untersucht wurden, wird dort nicht erwähnt. Man findet diese nur im ergänzenden Material. Es sind die folgenden (in den Klammern die Anzahl der Studien): Mit Zulassung: Paliperidone – extended release (9), Quetiapine (3),Aripiprazol (2), Asenapine (6),Lurasidone (6), Cariprazine (4), Brexpiprazol (3). Ohne Zulassung: Iloperidone (2), Bitopertin (1) – zurückgezogen, Bifeprunox (4) – Forschung aufgegeben, Blonaserin (1), Vabicaserin (1), LY2140023 (2), T-type calcium channel antagonist MK-8998 (1), BL-1020 (1), ITI-007 (1)AZD8529 (1) – keine Verbesserung, AZD2624 (1) – keine Verbesserung, Dopamine stabilizer RP 5063 (1), mGLU2/3 (1), pf-00217830 (1), Application number 21-436 (1). Für die meisten existiert nur eine Studie mit diversen Mängeln in der Qualitätsbewertung.
Die Publikation will den Zugang zu diesen Informationen offensichtlich erschweren, obwohl sie von erheblicher Bedeutung ist. Alle ausgewerteten und zugelassenen Substanzen haben eine nachgewiesenermaßen geringere Wirkung im Vergleich den 4 häufig verwendeten SGA. 15 Substanzen haben eine Zulassung gar nicht erreicht. Man kann von diesen Substanzen daher wohl keine bessere Wirksamkeit annehmen, um metaanalytisch eine insgesamt bessere Wirksamkeit als in der Publikation von 2009 nachzuweisen. Wären diese neuen Substanzen gut wirksam, wären sie sicher weiter beforscht worden. Sogar bei minder wirksamen ist dies erfolgt: Lurasidon, Asenapin, Caripiprazin.
Es ist also keineswegs glaubhaft, dass der Einschluss alter, qualitativ mäßiger bis schlechter Studien, sowie neuerer Einzelstudien nicht zugelassener Substanzen, in denen oft nur Wirkungen ohne Verringerung psychotischer Symptome ermittelt werden, tatsächlich eine verbesserte Wirksamkeit der Neuroleptika begründen könnte. Wo man Müll hineintut, kommt Müll heraus: ‚garbage in and garbage out‘.
Zusätzlich bestehen viele weitere methodische Einschränkungen, wie sie in allen pharmakologischen Studien zu Neuroleptika üblich sind, jedoch selten erwähnt werden.
(8) Die sog. ‚Placebo-Gruppe‘ besteht seit langem in allen Studien aus vorbehandelten Patienten (Ausnahme: die oben erwähnte Studie von Wang et al 2013 zu Ersterkrankten), oft über viele Jahre, die sich entschließen, an der Studie teilzunehmen und dann durch den Zufall der sog. Placebo-Gruppe zugeteilt werden. Dann wird bei ihnen das zuvor eingenommene Medikament fast immer in wenigen (2-5) Tage abrupt abgesetzt. Das ist auch in den hier ausgewerteten Studien so: „Die minimale Auswaschdauer betrug in der Regel nicht mehr als ein paar Tage.“ [„The minimum duration of washout was usually not more than a few days.“] (Leucht et al 2017)
Ein Anteil dieser Menschen entwickelt in wenigen Tagen bis Wochen Absetzphänomene, die oft über Wochen und Monate fortbestehen und sich langsam – und auch nicht immer vollständig – zurückbilden. Auch psychotische Symptome gehören zu diesen Absetzphänomenen, die oft als Rückfall bewerten werden und auch zum Abbruch der Studie führen können. „Psychotische und andere Verhaltenssymptome, die jedoch nicht immer von der ursprünglichen psychotischen Störung unterschieden werden können. Sie entstehen meist innerhalb von Tagen bis ungefähr sechs Wochen nach der Reduktion und bessern sich oftmals erst nach Wochen. Insbesondere Clozapin sollte nur langsam reduziert und abgesetzt werden, da hier ein erhöhtes Risiko für einen Rebound angenommen wird.“ (S 3 Leitlinie Langfassung S. 62)
Die Nachwirkung der Gabe von Antipsychotika VOR Umstellung auf Placebo in den Placebogruppen der placebokontollierten Studien und die Absetzeffekte zeigen sich eindeutig, wenn man sich die Verläufe der „Nebenwirkungen“ in den Placebo-Gruppen anschaut: Extrapyramidale Symptome und Verwendung von anticholinergen Medikamenten trat zwar häufiger in der Antipsychotikagruppe (19%), aber auch in der Placebogruppe (10%) auf, Dasselbe gilt für andere Nebenwirkungen. Wir wissen aber, dass Placebo KEINE extrapyramidalen Nebenwirkungen hervorruft!!! Entweder sind die Instrumente zur Erfassung von Wirkung und Nebenwirkung untauglich oder es sind eben die beschrieben spill-over-Effekte bzw. Entzugs- und Absetzeffekte, die wiederum die Studien kaum interpretierbar machen.
Diese Phänomene werden in den Mata-Analysen von Leucht und Kollegen überhaupt nicht diskutiert, obwohl sie einen Großteil der Studien infrage stellen.
Die vielfältigen Entzugsphänomene finden Sie auf Folie 30 der angehängten Leitlinien-Empfehlungen und selbstverständlich auch im Gesamttext auf S. 62 der Langfassung. Damit werden nun endlich Entzugsphänomene nach einer Neuroleptika-Einnahme in Leitlinien aufgenommen und nicht mehr in Abrede gestellt.
(9) Da die mittlere Studiendauer in der Metaanalyse nur 6 Wochen betrug – („Die mediane Studiendauer mit verwertbaren Ergebnissen betrug 6 Wochen (Bereich 3–28 Wochen; für den primären Endpunkt dauerten alle bis auf eine Studie 12 Wochen“) – müssen viele Abbrecher (Mittelwert von 37%) noch früher aus der Studie ausgeschieden sein. Da psychotische Entzugsphänomene oft 4-6 Wochen anhalten, sind viele bis dahin noch nicht abgeklungen, und werden fälschlicherweise als erneute oder unzureichend behandelte Psychose gewertet. Durch die Auswertungsmethode der Fortschreibung der zuletzt gemessenen Symptomatik der Abbrecher auch für spätere Messzeitpunkte (LOCF), werden psychotische Absetzphänomene, die noch nicht abgeklungen sind, dauerhaft als unzureichend behandelte Psychose gewertet. Es ist anzunehmen, dass dies eine verfälschende Bedeutung für das Gesamtergebnis hat, indem die Symptomlast der sog. Placebogruppe zu negativ bewertet wird. Bei einer NNT von 5 oder 6 können so auch psychotische Entzugsphänomene bei einem kleineren Teil der Patienten das Gesamtergebnis deutlich zu verfälschen.
Und was sagt eine Studiendauer von 6 Wochen mit einer die hohe Abbruchquote von 37% über die Chancen der Anwendung von Neuroleptika im Alltag aus? Und wie lassen sich damit Schlussfolgerungen und Empfehlungen für eine längere Anwendung überhaupt aussprechen? Damit ist also die „externe Validität“ sehr eingeschränkt, die Möglichkeit aus den Ergebnissen dieser Studien sinnvolle Schlussfolgerungen für eine Anwendung bei üblichen psychiatrischen Behandlungen zu ziehen.
(10) Methodische Einschränkungen durch mangelhafte Verblindung kommen noch hinzu und sind erheblich: Dazu aus dem Publikationstext: “In den Berichten wurden häufig keine vollständigen Details zur Sequenzgenerierung oder zum Verbergen der Zuordnung angegeben. Auch die Beschreibung der Methoden und des Erfolgs der Verblindung reichte häufig nicht aus.“ [„the reports often did not indicate full details about sequence generation or allocation concealment. Descriptions of the methods and success of blinding were frequently in- sufficient as well.] Behandler und Auswerter wissen in der Regel, wer Placebo und wer Antipssychotika einnimmt. Auch wissen sie meist, wer ein älteres Antipsychotikum (wie Haloperidol) oder ein „neueres“ einnimmt. So kann und wird die Wirksamkeit von Antipsychotika oft erwartungskonform eingeschätzt: Verbesserungen in der Placebo-Gruppe werden oft als geringer eingeschätzt und Verbesserungen in der Medikationsgruppe höher.
Und die folgenden Angaben macht Metaanalyse zu den Anteilen der Studien, in denen unterschiedliche Verzerrungen (‚risk of bias‘) möglich sind.
· Zufallsgenerierung: [„Random sequence generation: selection bias“]: Unklar bei 75% der Studien,
· Geheimhaltung der Zuweisung: [„Allocation concealment: selection bias“]: Unklar bei 75% der Studien,
· Verblindung des Teilnehmers und des Personals: [„Blinding of Participant and personal: performance bias“] – Unklar bei 50% der Studien,
· Verblindung der Datenerhebung: [„Blinding of assessment: detection bias“] Unklar bei 50% der Studien,
· Unvollständige Ergebnisdaten: [„Incomplete outcome data: attrition bias“] Hohes Risiko bei 40% der Studien, unklar bei 30%,
· Selektive Berichterstattung: [„Selective reporting“]: Hohes Risiko bei 50% der Studien, unklar bei 15%.
(11) In pharmakologischen Studien werden für diese Patienten unter „Placebo“ auch keine besonderen therapeutischen Angebote vorgehalten. Es besteht ja möglichst Verblindung. Dass diese existieren und sie die Rückbildung der Symptome auch ohne Neuroleptika verbessern, wissen wir aus der psychosozialen Psychosenforschung. Welche Kompetenzen und Möglichkeiten die behandelnden Teams der Studien haben, wird ebenfalls so gut wie nie berichtet.
(12) Keine Erhebung zur Befähigung im Alltag und in Beziehungen (Recovery)
Bei fast allen Studien zur Wirksamkeit von Antipsychotika wurde nicht gemessen, inwiefern Antipsychotika bei der Verbesserung des sozialen Funktionsniveaus, bei der Wiedereingliederung in den Alltag oder den Beruf oder bei der Verbesserung der sozialen Beziehungen halfen oder behinderten. Diese Zielgrößen sind letztlich jedoch die relevanten. Eine neuere Studie aus den Niederlanden (Wunderink et al 2013) zeigte erstmals, dass bei remittierten Patienten eine frühe und fortgesetzte Dosisreduzierung (die erzielte Dosis lag bei 2,2 mg anstatt bei 3,6 mg Haloperidol-äquivalenten) und ein Absetzen der Medikation in 21% der Fälle – unter therapeutischer Begleitung durch ambulante multiprofessionelle Teams – zu einer mehr als doppelt so hohen Recoveryrate (alltagsrelevante Funktionsfähigkeit) von 40,4% führte. Diese Fragestellung war nie zuvor untersucht wurden.
D. Was bedeutet das nun?
Als verlässlichster Ausgangspunkt sind also nur die Ergebnisse der Metaanalyse von 2009 ernst zu nehmen (Leucht, S. Arbter D, Engel RR, Kissling W, Davis JM (2009) How effective are second-generation antipsychotic drugs? Molecular Psychiatry 14: 429-47). Nur 41% unter Medikation hatten eine minimale Symptomreduktion. In dieser ist die Differenz in der Ansprechrate zwischen Medikation (41%) und Placebo (24%) nur 17%. Die Metaanalyse von 2017 steigert diese Ergebnisse ungerechtfertigt, durch Auswertung weiterer, methodisch mangelhafter oder undurchsichtiger Studien auf 51%.
Zu berücksichtigen ist jedoch, dass diese 41% insgesamt im Durchschnitt nur eine Verbesserung von 10 PANSS-Punkten erreichten, also nur 10 von 15 PANSS-Punkten, die einer minimal klinisch bedeutsamen Verbesserung entsprechen würden (also nur 66% der geringsten klinisch bedeutsamen Wirkung zeigten). In nordamerika-nischen Zulassungsstudien (Khin et al 2012) werden nur noch 6 von 15 PANSS-Punkten = 40% erreicht.
Bei Berücksichtigung einer klinisch angemessenen Wirksamkeitsschwelle von 25% Symptomreduktion läge demnach der Anteil von Patienten mit klinisch bedeutsamen Effekten deutlich unter 41%, etwa bei 38%.
ZUSAMMENFASSUNG
Aufgrund von erheblichen methodischen Mängeln der Metaanalyse von 2017 und die dadurch notwendigen Korrekturen verringert sich also ermittelte minimale Response (niedrigste klinische noch bedeutsame Symptomreduktion) von 51 % auf nur etwa 38%, und damit auch der Unterschied zwischen den Studiengruppen unter Medikation und unter Placebo (mit 22%) von 21% auf etwa 16%.
So sinkt der Anteil der Menschen, der tatsächlich und auch nur geringfügig von Neuroleptika profitiert, auf etwas mehr als ein Drittel (38%) mit einer NNT von 6. Und nur bei weniger als einem Viertel (23%) der Behandelten zeigt sich eine Symptomreduktion um 50 % mehr, was angesichts der Placeborate lediglich eine NNT von 10 bedeutet.
Dabei ist die NNT (‚number needed to treat‘) – die Anzahl der notwendigen Behandlungen – eine statistische Maßzahl, die angibt wie viele Patienten pro Zeiteinheit (hier durchschnittlich 6 Wochen, länger wurden die Studien im Mittel nicht durchgeführt und in diesem Zeitraum betrug durchschnittliche Abbruchquote 37 %) mit dem Medikament behandelt werden müssen, um das gewünschte Therapieziel bei einem Patienten zu erreichen.
Würden auch alle weiteren methodischen Einschränkungen berücksichtigt, sinkt die tatsächliche Wirksamkeit noch weiter ab.
Aber was bedeutet dies nun für die Mehrheit der Patienten, wenn alle in der gleichen Weise behandelt werden? Wenn weniger als 17% eine nur minimale klinisch bedeutsame Wirkung gegenüber einem Scheinmedikament erleben, werden viele ohne Nutzen mit Substanzen behandelt, an denen sie subjektiv oft erheblich leiden, die sie oft erheblich körperlich schädigen, oftmals irreversibel. Fast regelhaft kommt es bei der unzureichenden Wirksamkeit zu weiteren Dosissteigerungen ohne klinischen Vorteil, jedoch oft mit zunehmenden Nebenwirkungen und ohne Korrektur oder Absetzversuche im Verlauf, was diese Leitlinien erstmals empfehlen. Die psychischen Funktionen der so Behandelten, die erforderlich sind für ihren Genesungsprozess, werden durch Fehl- oder Überdosierungen weiter geschwächt. Das körperliche Abhängigkeitspotential der Neuroleptika ist bis heute völlig unzureichend erforscht, lässt sich jedoch durch langfristig gelungene Absetzprozess belegen. Auch stehen bis heute gute Studien aus, die gesichertes Wissen zu Absetzprozessen zur Verfügung stellen können.
Der Versorgungsalltag ist so unflexibel, dass die Akteure bei psychotischen Symptomen reflexhaft zu Neuroleptika greifen, und gar keine anderen Optionen kennen und zur Verfügung haben. Echte Alternativen stehen nicht zur Verfügung, auch wenn darüber aufgeklärt werden soll. Das führt zu mehr Druck auf Patienten, bis hin zu Menschenrechtsverletzungen.
Die steigende Placebo-Response bei besserer klinischer Versorgung und spezifische Ansätze (Soteria, Bedürfnisangepasste Behandlung, Offener Dialog) weisen jedoch den Weg. Durch Rezeptorveränderungen infolge der pharmakologischen Behandlung ist das wieder Absetzen erschwert und Entzugsphänomene sind oft so ängstigend, muten wie Rückfalle an und sind auch tatsächlich oft schwer davon zu unterscheiden. Wie es trotzdem möglich ist, hat erst die internationale Betroffenenbewegung herausgefunden. Nun endlich haben diese Erkenntnisse, in Verbindung mit viel zu spät begonnener und noch sehr unzureichender Forschung, Eingang in diese Leitlinien gefunden.
E. Vergleich von sogenannten „Atypika“ (SGA) und „Typika“ (FGA)
In diesen Leitlinien wird keine bevorzugte Empfehlung mehr für FGA (ehemals Typika) oder SGA (ehemals Atypika) ausgesprochen. Einzig und allein das individuelle Nebenwirkungsprofil bei jeder Patient*in soll das wichtigste Entscheidungskriterium sein. Und dies bevorzugt keine Substanzklassen. Dies ist eine fast unbemerkte Beerdigung 2. Klasse für einen Marketing-Trick, mit dem Pharmaindustrie über mehr als 10 Jahre viele Milliarden Gewinne gemacht hat und der einigen Psychiater eine gutes Zusatzeinkommen möglich gemacht hat. Erst durch diese unkritischen, an Drittmitteln der Industrie und persönlichen Honoraren interessierten Psychiater, konnte dieses Marketing Glaubwürdigkeit erlangen.
Psychiater und Studienautoren, auch anscheinend unabhängige Reviewer wie Prof. Leucht, haben sicher gute Gründe, die Anwendung von SGA zu verteidigen. Letztgenannter hat beispielweise erhebliche Interessenskonflikte. 2012 schrieb er: “In the past 3 years Stefan Leucht has received fees for consulting and/or lectures from the following companies: Bristol-Myers Squibb, Actelion, Sanofi-Aventis, Eli Lilly, Essex Pharma, AstraZeneca, MedAvante, Alkermes, Janssen/Johnson & Johnson, Lundbeck Institute and Pfizer, and grant support from Eli Lilly. W.K. has received fees for consulting and/or lectures from Janssen-Cilag, Sanofi-Aventis, Johnson & Johnson, Pfizer, Bristol-Myers Squibb, AstraZeneca, Lundbeck, Novartis and Eli Lilly.” Und 2017 “In the last 3 years Dr. Stefan Leucht has received honoraria for consulting from Roche, TEVA, Otsuka, Lundbeck, and LB Pharma; for lectures from Otsuka, Lundbeck, Janssen, ICON, Lilly, SanofiAventis, AOP Orphan, Roche, and Servier; and for a publication from Roche.”
Obgleich die Reviews keine Überlegenheit neuerer gegenüber älteren Antipsychotika zeigen, wurde von diesen Reviewern dieser Mythos, auch derjenige einer niedrigeren Rate an Nebenwirkungen, lange Zeit aufrechterhalten. Dies erfolgte durch Nicht-Berücksichtigung methodischer Einschränkungen der Studien (und damit auch der Meta-Analysen) die sich zu Ungunsten der Antipsychotika (gegenüber Placebo) oder zu Ungunsten neuerer gegenüber älteren Antipsychotika auswirken würden, durch zu positive Schlussfolgerungen, durch die Nutzung schwer verständlicher statistischer Methoden etc. Damit nutzen sie zum Teil ähnliche Mechanismen wie diejenigen der Hersteller der Medikamente .
So ist es gelungen den Mythos der Atypika so lange aufrecht zu erhalten, um die patentgeschützte hochpreisige Gewinnabschöpfungsphase abzusichern. Es ist gut für diese Industrie, dass sich auch heute noch genügend Wissenschaftler und Psychiater finden lassen, die sich die Bewerbung aktuell teurer Depot-Präparate „moderner“ Substanzen und neuerer Substanzen ohne echtes Innovationspotenzial und mit schlechten Ergebnissen wie Cariprazin bezahlen lassen.
F. Vergleich der Antipsychotika mit Medikamenten in der somatischen Medizin anhand der Kennzahl „Number Needed To treat“ (NNT, Anzahl der notwendigen Behandlungen)
Die doch ernüchternde Anzahl der notwendigen Behandlungen (NNT) von Neuroleptika wurde mit der Wirksamkeit von Medikamenten (als NNT) in der Somatik verglichen. (Leucht et al 2012) Bei einem solchen Vergleich seien sie im Allgemeinen nicht weniger wirksam als diese Medikamente.
Ausgewertet wurden: Aspirin (Prävention Schlaganfälle), Antihypertensiva, ACE Hemmer, Statine, Migränemittel, Metformin (Diabetes), Protonenpumpenhemmer (Ösophagitis), Antibiotika, Chemotherapeutika, Interferon (Hepatitis), Thrombolyse (Schlaganfall), Corticosteroide (Rheumatoide Arthritis). Es sind also meist gut verträgliche Mittel zur langfristigen Prävention oder kurzfristigen Akutbehandlung oder Medikamente bei tödlich verlaufenden Erkrankungen oder zur Verhinderung schwerer und eindeutig definierter und messbarer medizinischer Ereignisse wie Herzinfarkt, Schlaganfall, andere kardiovaskuläre Ereignisse und Tod.
Im Gegensatz dazu basiert die Wirksamkeit von Neuroleptika ausschließlich auf subjektiven Einschätzungen von oft nur geringen oder keinen Symptomabschwächungen und einer „Rückfallverhütung“.
Neuroleptika haben auch häufiger und oft schädlicherer Nebenwirkungen, als die mit ihnen verglichenen Medikamente für somatische Erkrankungen. Die Autoren haben jedoch Nebenwirkungen nicht in den Vergleich mit einbezogen. „Es wäre einfach unmöglich gewesen, Nebenwirkungen ebenfalls zu beschreiben und sie gegen die Wirksamkeit abzuwägen, denn es gibt viele subjektiv urteilende Aussagen.“ (Leucht et al 2012) [It would have been simply impossible to describe side-effects a s well and to balance them with efficacy, because there are many subjective judgement calls.“] Aber sie gestehen zu, dass diese ernstes Problem vieler Psychopharmaka seien, obwohl Verbesserungen gemacht wurden .
Anders als in der Somatik werden Patienten in der Psychiatrie jedoch recht oft zur Einnahme von Neuroleptika gedrängt und genötigt und oft keine Alternativen angeboten.
Die weiterhin propagierte pharmakologische Dominanz behindert seit Jahrzehnten die Entwicklung von regionalen und schnell zugänglichen Alternativen oder kompetenten und ausreichend kontinuierlichen psychotherapeutischen und psychosozialen Behandlungen.
All dies muss mit bedacht werden, anstatt mit dem Hinweis auf die Somatik ein Gefühl des ‚gut genug‘ zu entwickeln.
Der Hinweis auf die Somatik kann auch nicht ausreichen, denn viele Patienten und auch Angehörige fordern Alternativen, wollen wissen, ob die Medikation, die sie jahrelang oder lebenslang einnehmen sollen, überhaupt so wirksam ist, um dies zu rechtfertigen Das gesamte Paradigma und die alten Denk- und Handlungsgewohnheiten müssen daher zunehmend in Frage gestellt werden.
F. Literatur
Ausgewertete Metaanalyse:
Leucht S, Leucht C, Huhn M, Chaimani A, Mavridis D, Helfer B, Samara M, Rabaioli M, Bacher S, Cipriani A, Geddes JR, Salanti G, Davis JM. (2017) Sixty Years of Placebo-Controlled Antipsychotic Drug Trials in Acute Schizophrenia: Systematic Review, Bayesian Meta-Analysis, and Meta-Regression of Efficacy Predictors. The American journal of psychiatry. 174 (10): 927-42. Diese Publikation ist die Nummer (185) in der Literaturliste der Leitlinien.
Volltext frei:https://ajp.psychiatryonline.org/doi/pdfplus/10.1176/appi.ajp.2017.16121358
Suppl.Material https://ajp.psychiatryonline.org/doi/suppl/10.1176/appi.ajp.2017.16121358/suppl_file/appi.ajp.2017.16121358.ds001.pdf
Weitere:
Bola JR, Kao DT, Soydan H (2011) Antipsychotic medication for early episode schizophrenia. Cochrane Database of Systematic Reviews CD006374
Volltext frei: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4105695/
Danborg & Gøtzsche (2019) Benefits and harms of antipsychotic drugs in drug-naive patients with psychosis: A systematic review. International Journal of Risk & Safety in Medicine 30(4):193‑20
Volltext frei: https://www.ncbi.nlm.nih.gov/pubmed/?term=Benefits+and+harms+of+antipsychotic+drugs+in+drug-naive+patients+with+psychosis%3A+A+systematic+review.
Grams HA (2005) Die Relevanz medizinischer Leitlinien nimmt zu, Deutsches Ärzteblatt, 102 (12):814‑816 https://www.aerzteblatt.de/archiv/46031/Arzthaftungsrecht-Die-Relevanz-medizinischer-Leitlinien-nimmt-zu
Guillin, O, Abi-Dargham A., Laruelle M. (2007) Neurobiology of dopamine in Schizophrenia. International Review of Neurobiology 78: 1-38
Abstract: https://www.ncbi.nlm.nih.gov/pubmed/17349856
Howes OD (2012): The Nature of Dopamine Dysfunction in Schizophrenia and What This Means for Treatment Arch Gen Psychiatry 69(8):776-86.
Volltext frei: https://www.ncbi.nlm.nih.gov/pubmed/?term=Schizophrenia%3A+an+integrated+sociodevelopmental-cognitive+model
Howes OD & Murray RM.(2014) Schizophrenia: an integrated sociodevelopmental-cognitive model. Lancet. 383(9929):1677-1687.
Volltext frei: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4127444/
Khin Ni A et al (2012) Exploratory Analyses of Efficacy Data From Schizophrenia Trials in Support of New Drug Applications Submitted to US Food and Drug Administration, J Clin Psychiatry 73(6): 856‑864
Abstract: https://www.psychiatrist.com/JCP/article/Pages/2012/v73n06/v73n0620.aspx
Leucht S, Kane JM, Etschel E, Kissling W, Hamann J, Engel RR (2006) Linking the PANSS, BPRS, and CGI: clinical implications. Neuropsychopharmacology 31(10): 2318–2325
Volltext frei: https://www.nature.com/articles/1301147.pdf
Leucht, S. Arbter D, Engel RR, Kissling W, Davis JM (2009) How effective are second-generation antipsychotic drugs? Molecular Psychiatry 14: 429-47
Volltext frei: https://www.nature.com/articles/4002136.pdf
Leucht S, Leucht C, Huhn M, Chaimani A, Mavridis D, Helfer B, Samara M, Rabaioli M, Bacher S, Cipriani A, Geddes JR, Salanti G, Davis JM. (2017) Sixty Years of Placebo-Controlled Antipsychotic Drug Trials in Acute Schizophrenia: Systematic Review, Bayesian Meta-Analysis, and Meta-Regression of Efficacy Predictors. The American journal of psychiatry. 174(10):927-42. https://ajp.psychiatryonline.org/doi/full/10.1176/appi.ajp.2017.16121358
Leucht S, Hierl S, Kissling W, Dold M, Davis JM.(2012) Putting the efficacy of psychiatric and general medicine medication into perspective: review of meta-analyses. Br J Psychiatry.200(2):97-106.
Abstract: https://www.ncbi.nlm.nih.gov/pubmed/?term=)++Putting+the+efficacy+of+psychiatric+and+general+medicine+medication+into+perspective%3A+review+of+meta-analyses
Rief, W., Barsky, A. J., Bingel, U., Doering, B. K., Schwarting, R., Wöhr, M., & Schweiger, U. (2016). Rethinking psychopharmacotherapy: The role of treatment context and brain plasticity in antidepressant and antipsychotic interventions. Neuroscience and Biobehavioral Review, 60, 51‑64.
Volltext frei: https://reader.elsevier.com/reader/sd/pii/S0149763415300804?token=BDE276376F3C87966C0B83A42B2646A9CF6779B82BA2AB5993F9F1E433A99B78B714C8A5DC77D896D49D2FDD6E281576
Trikalinos TA, Churchill R, Ferri M, et al: (2004) Effect sizes in cumulative meta-analyses of mental health randomized trials evolved over time. J Clin Epidemiol 57:1124‑1130
Abstract: https://www.sciencedirect.com/science/article/abs/pii/S0895435604001258
Wang C-H, Li Y, Yang J, Su L-S, Geng Y-G, Li H, et al. (2013) A randomized controlled trial of olanzapine improving memorydeficits in Han Chinese patients with first-episode schizophrenia. Schizophr Res. 144:129-35
Abstract: https://www.sciencedirect.com/science/article/abs/pii/S092099641300008X
Wunderink L, Nieboer RM, Wiersma D, Sytema S, Nienhuis FJ (2013) Recovery in remitted first-episode psychosis at 7 years of follow-up of an early dose reduction/discontinuation or maintenance treatment strategy: long-term follow-up of a 2-year randomized clinical trial. JAMA Psychiatry. 70(9):913-20
Volltext frei: https://jamanetwork.com/journals/jamapsychiatry/article-abstract/1707650
Von Dr. Volkmar Aderhold und Dr. Dr. Stefan Weinmann